緊急使用授權
」 高端 疫苗 EUA 高端疫苗 快篩
新冠迎流行期!估7月單周就醫破10萬人次 莊人祥:不恢復口罩令
新冠疫情再起,疾管署預估,這波疫情高峰將落在7月中旬,屆時每周約有1千例中重症住院個案,若包含輕症個案,每周門急診就醫可能超過10萬人次。醫師表示,夏天仍有疫情上升,這和冠狀病毒不停突變有關,由於人體對新變異株抵抗力較低,就可能二次感染。疾管署長莊人祥表示,不會恢復強制戴口罩措施,但建議民眾前往人潮眾多場所時戴上口罩。國內再度進入新冠流行期,衛福部長邱泰源27日表示,「防疫體系還在」,因應新冠疫情上升,正積極進行4大策略,包括密切監測國內外疫情、強化防疫物品儲備和調度、訂定相關指引、加強衛教以及醫療院所合作。邱泰源指出,已提供300萬劑家用快篩試劑供基層醫療院所發放,並積極儲備新冠抗病毒藥物。莊人祥說明,國內瑞德西韋庫存量尚可使用159天,倍拉維96天、莫納皮拉韋17天,並已完成2萬人份莫納皮拉韋採購,預計7月4日抵台。莊人祥提到,莫納皮拉韋預防重症效果較倍拉維差,目前被列為「有條件下使用」,全球僅日本給予藥證,在台灣仍屬緊急使用授權(EUA),今年底就會屆效。待EUA失效或庫存用完後,莫納皮拉韋將逐漸過渡到其他用藥,例如美國FDA和我國食藥署正在審查倍拉維用於重度腎功能不全及透析患者。莊人祥表示,這是Omicron第6波疫情,已經超過今年初的第5波高峰,目前還在上升,但預估不會超過去年的第4波疫情。國內上周新冠併發症個案共817例、健保門急診新冠陽性約9萬人次,預估會在7月中旬達到疫情高峰,屆時每周併發症個案超過千例,包含輕症在內,可能超過10萬人次就醫。台大醫院小兒感染科醫師李秉穎預估,這一波疫情應和今年1、2月的疫情差不多,不可能回到過去的大規模流行,而是像季節性流感一樣,「以前是大海嘯,現在是小波」。至於口罩令是否可能重啟?莊人祥說,新冠肺炎已經不是第五類法定傳染病,過去強制戴口罩措施已無法源,因此不會恢復相關規定,但仍建議前往人潮擁擠處戴口罩,各醫院也可以自行規定是否要求民眾戴口罩。中國醫藥大學附設醫院感染管制中心副院長黃高彬則建議60歲以上的民眾,在人多或密閉空間,或搭乘大眾運輸工具時,都要把口罩戴好。

新冠又開始流行了!疫情預計7月達高峰 疾管署:上周門急診破9萬人次
新冠疫情再起,預計7月中旬到達高峰,衛福部長邱泰源今天親自坐鎮疾管署召開記者會,強調「防疫體系還在」,多項防疫策略都在積極進行。疾管署長莊人祥說,上周健保門急診診斷新冠陽性約9萬人次,到了高峰期可能超過每周10萬人次,但由於已無適法性,不會恢復強制戴口罩的措施。近期有醫師反映新冠抗病毒藥物莫納皮拉韋(Molnupiravir)缺貨,莊人祥說明,目前莫納皮拉韋仍有8000多人份,雖然今年3月衛福部傳染病諮詢委員會已決議原則上不再採購,但因應使用需求和疫情上升,已完成2萬人份採購作業,另有2萬人份的開口合約。不過莊人祥提到,莫納皮拉韋在臨床上和WHO都列為「有條件下使用」,全球僅日本給予藥證,在台灣仍屬於緊急使用授權(EUA),今年底就會屆效,待EUA失效或庫存用完後,將逐漸過渡到其他用藥,例如美國和我國食藥署正在審查倍拉維(Paxlovid)用於重度腎功能不全及透析患者。莊人祥提到,莫納皮拉韋預防重症效果只有3成多,倍拉維則有7成多。但臨床上有些醫師或患者擔心倍拉維的交互作用,因此希望開立莫納皮拉韋,莊人祥表示,相信醫師臨床上都有裁量,疾管署也和醫師公會溝通,未來在病例中加入開立莫納皮拉韋的理由,未來會做評估,讓大家更謹慎開立這個藥物。疾管署27日舉行「COVID-19抗病毒藥物處置議題」臨時記者會,衛福部長邱泰源(見圖)出席。(圖/中國時報記者劉宗龍攝)莊人祥也分享自己高齡9旬母親的經驗,當時使用心律調整器、抗凝血劑、心臟病和降血脂藥物,剛好都是倍拉維的使用禁忌,當時他也認為只能用莫納皮拉韋,但經過和醫師討論,由於倍拉維的療效較好,醫師認為只要慢性病藥物暫停幾天就好,最後開立了倍拉維,讓媽媽順利康復。另外,有部分縣市傳出倍拉維也缺貨,莊人祥強調,國內至少還有3個月用量,今年9月以前還會再來一批。目前倍拉維已取得藥證,屬於處方用藥,民眾如有自費需求,亦可請醫師開立處方箋,向該公司通路購買。近期疫情上升,預估在7月中旬達到高峰。莊人祥指出,這是Omicron第六波疫情,已經超過今年初的第五波的高峰,目前還在上升,但預估不會超過去年的第四波。國內上周併發症住院個案約800多例,預估在高峰時會達到每周1000多例,至於整體感染個案,上周健保門急診診斷新冠陽性約9萬人次,到了高峰期可能超過10萬人次,提醒高風險病人及早就醫並使用口服抗病毒藥物。至於口罩令是否可能重啟?莊人祥說,目前疾管署建議進醫院戴口罩,先前強制戴口罩是因為第五類傳染病,但現在已經沒有了,因此不會恢復到過去的強制措施,但各醫院可以自行規定是否要求民眾入內須戴口罩。

一滴現形1/台南囡仔勇闖美國FDA 瑞磁自創全球唯一液態晶片「病毒無所遁形」
「每個醫生聽到我的點子後,都說要做、這對病人來說非常重要,但科學家朋友們都叫我不要做,因為實在太難了!」今年70歲的瑞磁生物科技集團ABC-KY (6598)創辦人何重人說。在一個陽光耀眼的午後,何重人在內湖的辦公室接受CTWANT記者專訪,內湖的辦公室很簡約,大螢幕投射的是他所發明的數位生物條碼(BMB)的介紹,一般人可能不太容易聽懂,他耐心解釋,就像個大學教授;他成功在美國拿到FDA認證的多元診斷試劑,已可驗出78種疾病,但他不滿足於年年擴增的「產品菜單」,想要挑戰下一步,就是由一滴血液,來判讀癌症患者是否會復發。瑞磁生技美國子公司Applied BioCode 於2008年在美國洛杉磯成立,2015年在台北設點,創辦人何重人是不折不扣的台灣人,1954年在台南出生,自中興大學化學系畢業後,到美國亞利桑那州立大學念生化碩士、物理化學博士,當過紐約哥倫比亞大學博士後研究員。他笑說,就是讀書讀太久,後來找工作總想找符合專業和喜好,挑來挑去選不到喜歡的,幸好美國創業風氣盛,只要有新點子就能獲得啟動資金,他在2008年成立Applied BioCode,經過十年研發和打磨,終於在2018年取得FDA(美國食品藥物管理局)自動化分子診斷系統的上市許可,同年還取得17項腸炎檢測試劑,2019年則拿到呼吸道20項體外診斷試劑的上市許可。瑞磁2018年取得17項腸炎檢測試劑、2019年拿到呼吸道20項體外診斷試劑的FDA上市許可。(圖/瑞磁提供)自嘲在「在學校待太久」的何重人,在化學、物理、光學與生物技術等跨領域累積豐富知識,加上出自半導體強國台灣,因此想到半導體製程技術,採用6吋晶圓切割成300萬個磁珠,打造出細如塵埃的微小晶片,以QR code的形式黏在生物探針上,放置在特製的溶液試劑中,若檢體中出現相對應的細菌或病毒,就能被晶片上的生物探針抓住,在專門的機器拍攝下呈現不同色彩,這組BMB就可得知這次生病的「確切兇手」。「我們用QR code便宜又準確的優勢,縮小100萬倍來做,」何重人說,過去做生物檢測,一次只能一個人做一種,答案出來發現錯了,才能再試別種,所以大部分的人都不想花精力在這上面,然而他的創新作法,一次可確認或排除10多種病毒,一台機器更可在3.5小時,同時完成96人的檢體,可說是又快、又好、又便宜。以一個正在打噴嚏的病人為例,過去只能戳一次鼻子、驗一種病毒,就像我們平常驗新冠肺炎的方式,根本就不符合時間與成本效益,所以大部分都靠瞎子摸象,吃一般感冒藥去壓症狀,運氣好就見效,運氣不好反而延誤治療,現在有了這項新技術後,用棉花棒戳鼻子、放進試劑、拿去機器拍照,短時間內就能知道,到底是A型、B型流感、呼吸道融合病毒、人類間質肺炎病毒,還是新冠、腸病毒,甚至是百日咳桿菌、肺炎黴漿菌等都能測出,讓醫生對患者用藥做出正確判斷。瑞磁生技副總陳祐寧表示,目前有腸胃道檢測、呼吸道檢測、新冠與流感檢測等診斷試劑產品,均拿到美國FDA核可,最新推出的是多元真菌檢測,則是將傳統耗時2周以上的真菌培養再檢測,縮短到5個小時就能完成;接下來每年將陸續推出新品項,像是性傳染病與抗藥性基因檢測、泌尿道感染結合抗藥性基因檢測等。用瑞磁的技術,做一次鼻腔採樣,就能有7種不同的病毒檢測。(圖/翻攝自Applied BioCode官網)先前研究也發現,瑞磁的新冠加流感七合一檢測,一次上機做96個檢體僅23分鐘,而業界龍頭大約要花50分鐘,但檢測結果差異不大,所以在疫情期間瑞磁順利取得美國 FDA 緊急使用授權(EUA),且一次鼻腔採樣就能做到7種不同的病毒檢測,比業界龍頭更強。陳祐寧透露,美國當地醫院目前幫病人做檢測,大多採用亞培、羅氏等巨頭企業產品,雖然一次做一種,但在醫療保險支應下,美醫療業者不太容易改用新產品,不過,最近美國保險業開始有降低給付趨勢,台灣產品因性價比相對高,能提供醫院或實驗室彈性挑選檢測與出報告的項目,以符合保險給付上限,有望受到更多的青睞。由於傳染病、過敏原等檢測開發產品已上軌道,已交由團隊研發,何重人告訴記者,他現正研究如何透過血液變化、而非開刀取檢體的方式,探討癌症復發的可能性,進而做到早期發現、早期治療,「定時扎個血做檢查,就不需時時提心吊膽。」他期待地說。儘管沒有前例可循,科學家朋友也認為太過困難,不過何重人說,「在醫院看到很多患者與家屬,為了這難以根治的癌症腫瘤在憂慮,感覺很沉重。」如果這技術做出來能幫助很多人,讓他有持續做下去的動力。

細看高端合約「這2點」太詭異 賴士葆:這不是電影演的情節嗎?
副總統賴清德在競選時承諾公開高端疫苗合約,16日疾病管制署署長莊人祥公開高端的58頁合約。不過,國民黨立委賴士葆說,高端通過EUA(緊急授權),當天就改合約,希望衛福部能向大眾說明2疑點。而國民黨北市議員游淑慧也說,「高端疫苗EUA怎麼過的?到底要保密什麼?」賴士葆在臉書發文,「7/19通過EUA,7/19就立刻改合約,重新訂了更嚴格的保密合約,仔細看真是太詭異!」賴士葆說,「第一條就寫到合約簽署日之前或之後的資料都屬於機密資料。合約都還沒簽,資料就算機密?難道合約簽署之前就有不可告人的資料,所以連沒簽約之前的都不能公開?政府會不會對高端過度保護?」賴士葆表示,「第二條第五款提及,必須向法院或主管機關要揭露機密資料時,要先通知對方,並且盡力縮小揭露範圍。如果都遭受法院調查時還要先通報並且盡量隱匿?這不是電影才會演出的情節嗎?法院或主管機關如果都要調查了,還得預先通知資料提供者!是為了串供還是銷毀資料,必須說清楚!之前法院調查高端炒股案時,是否有依照合約通知?」賴士葆稱,高端多次延遲交貨,衛福部包庇不罰或輕罰,「衛福部絕對不可能發個新聞稿就想船過水無痕!必須針對以上的疑點向社會說清楚講明白,否則很難洗清外界對於衛福部處處為高端護航、有圖利高端之嫌的疑慮!」游淑慧指出,之前民進黨政府以保密條款為由拒公開,「原來,原本的合約是正正常常、沒有保密條款,但2021年7月19日突然進行契約變更,而唯一變更的內容,就是新增這個保密條款。」游淑慧,2021年7月18日食藥署邀專家開會,討論高端緊急使用授權,隔天衛福部正式核准高端專案,發了EUA,「為什麼在拿到EUA後,就趕快同時加上保密條款,高端疫苗EUA怎麼過的?到底要保密什麼?我想更重要的是當初的EUA審查資料,也應一併公開。」

高端好神1/還未EUA先製造375萬劑疫苗 民眾黨批:未卜先知草菅人命
高端疫苗採購疑雲持續延燒,民進黨總統候選人賴清德日前曾表態應公開高端疫苗合約,卻遲遲沒有下文,立法院也在9日召開臨時會邀請行政院長陳建仁專案報告,陳建仁強調絕無黑箱,不過民眾黨中央委員張凱鈞拿出一份機密文件,指控高端在通過二期試驗的半年前,就已大量生產總計375萬劑的疫苗原液,根本就是草菅人命。張凱鈞向本刊出示一份印有「機密資料,不得外流」的文件指出,那是高端疫苗開發推動情形二期試驗的內部資料,裡面清楚刊載,在生產計畫的執行情形中,已在2021年4月28日生產50L與200L的疫苗原液,總計375萬劑,但其二期試驗查核卻是在同年6月才完成,並將查核結果併入EUA(緊急使用授權)審查。張凱鈞指出,高端早在2021年4月就已生產50L與200L的疫苗原液,但其二期試驗查核卻在同年6月才完成,質疑高端「超前部屬」。(示意圖/與本案無關,報系資料照)張凱鈞怒控,高端2021年6月22日才完成二期試驗,而疫苗原液相關查核竟全數均由高端廠內自行檢驗,且7月中下旬專家會議才核准50L製成產品、同年10月中旬才獲得EUA核准200L製程產品,但高端卻已在半年前提早產出疫苗等著出貨,讓他忍不住痛批,為何高端可以一路綠燈未卜先知,在沒有得到核准許可前就大量生產疫苗原液,「這不是超前部署什麼叫做超前部署?」張凱鈞也拿出一段高端董監事會議流出的錄音檔表示,錄音內容談到「疫苗和新藥開發不一樣,疫苗是量的問題,新藥則是0和1的問題,癌症只有治療的好跟治療不好,疫苗是保護率幾%,60分和90分的問題,不是成敗一翻兩瞪眼的問題…疫苗就是安全有效…有效這條線怎麼劃,萬一假設不太理想…動物也是這樣啊,先做小劑量不夠再加大劑量。」 張凱鈞受訪時直言,高端竟然將動物比做人類,「不夠再加大劑量就好,現在已有300多萬劑疫苗打進人民身上,根本就是草菅人命」。他說,黨團收到的資料中,還有一段是高端在第二期試驗過程中,總計招募3852人進行試驗,未料在二期試驗實際送審中,高端疑似僅將1000名數據較好的資料送驗,好讓數據資料好看,「在學術界中根本聞所未聞。」張凱鈞痛批,為何高端可以一路綠燈未卜先知,「這不是超前部屬什麼叫做超前部屬?」。(圖/趙文彬攝)張凱鈞痛斥,高端後續就連發表論文都有疑慮,儘管其所發表的論文上有美國國衛院(NIH)掛名,但從董監事會議上流出的錄音卻顯示,NIH曾因認為其在論文裡貢獻度不夠而詢問高端董監事「我掛這個名是有什麼貢獻嗎?」委婉拒絕掛名,高端董監事卻回應「你掛名就是貢獻啊」,更表示「掛名對於登載一級雜誌會比較有幫助。」以此試圖讓高端走向國際,但事實是高端未能走向國際,更沒通過國際認證與三期試驗,還將疫苗銷毀160多萬劑。張凱鈞指出,高端曾在2021年2月向總統府報告,賴清德到底扮演何種角色?而高端在同年7月28日壓線通過EUA認證(效期1年),隔年就因九合一選舉,疑似為救陳時中選情,再次通過EUA認證,股價因此狂飆14倍,總統府是否真的沒有圖利?「公布合約還是其次,政府敢不敢公開二期試驗的送驗資料?」高端疫苗製程與二期試驗通過時間序對比之下就可看出問題。(圖/本刊繪圖組)

指高端契約只是冰山一角 柯文哲:若要公開就從頭公開
選舉進入倒數階段,高端疫苗爭議再起成為選舉攻防議題,立法院9日確定召開臨時會,要求行政院長陳建仁就高端合約公開事項到立院專案報告。民眾黨總統候選人柯文哲8日表示,高端疫苗問題不只在契約,還牽涉到EUA審查、採購過程,以及後續股票操作獲利等多層面。他認為,既然政府要公開,就從頭公開。柯文哲指出,所謂正常國家,首要條件就是人民信任政府,而高端疫苗事件卻嚴重傷害民進黨政府與國人之間的互信。他說,以他對民進黨的了解,一定有所準備,但問題不是企業契約,而是EUA(緊急使用授權)是如何通過、整個採購過程,以及後來的股票操作等,「契約只是冰山一角,看不到水面下的90%,那才是問題」。他認為,政府要全面公開這些資訊,包括股票操作和金流等,從頭到尾都應該一覽無遺。民眾黨立委賴香伶則指出,政府所提供的文件被要求保密30年,至140年的2月25日,這樣的措施實質上是封存,而非保存。她質疑,國會立委在調閱權時所獲取的資料多為塗黑的資訊,這種做法是否真正公開,是否能反映真相。賴香伶進一步提到,在衛環委員會的疫苗調閱小組中,她是最早揭露文件塗黑情況的立委之一。她認為,如果臨時會所獲取的資訊仍然是被塗黑的,這等於打假球,希望在最後一次臨時會中揭開真相。賴香伶呼籲民進黨黨團不要再護航,應從善如流,對於民眾對於疫苗採購真相的期待,不應再推遲。她希望政府能夠在最後一次臨時會中揭開黑箱,實現公開透明的政府,還給國人對於知道真相的權利。

民眾黨團支持召開臨時會 促公開高端疫苗合約內容
立法院長游錫堃8日上午召集朝野協商,針對是否加開臨時會邀行政院長陳建仁至立院報告高端案進行朝野協商。民眾黨團總召邱臣遠、副總召賴香伶、幹事長張其祿召開記者會,表達支持召開臨時會,也要求行政院長陳建仁到立法院進行專案報告,並盡速公布合約內容。邱臣遠強調,針對國產疫苗研發、採購及相關流程,以及藥害損害賠償等事宜,政府應該一併公開,因為這關乎國人的生命財產權益,必須正視「人民有知的權利」。邱臣遠表示,針對高端疫苗的爭議,他們拒絕黑箱作業,支持召開臨時會,公開高端採購合約內容。他指出,高端疫苗原本應是新冠疫情的「救命良藥」,但在整個採購過程中,民進黨政府不願公開透明,許多程序爭議至今未解。賴清德在選前才表態「贊成公開」,針對此事,在野黨倡議召開臨時會,應給全體國人一個交代。邱臣遠說,執政黨不應該忽視民意,最令國人關心的問題,包括高端採購合約內容、EUA的申請過程、高端股價是否異常波動、是否有人藉機發國難財等,執政黨都應該對國人公開透明,民主台灣拒絕政府進行黑箱作業。賴香伶表示,高端爭議多不勝數,時任指揮中心發言人莊人祥2021年6月13日說,若等解盲通過才下訂簽約,將無助防疫,然而莊人祥完全忽略風險問題,對程序瑕疵更不願多作解釋,政府在高端二期還沒解盲就先簽採購合約,解盲記者會當天上午,衛福部才公布緊急使用授權(EUA)審查標準,根本就是「先射箭再畫靶」,令社會大眾難以信服。張其祿直言,審計部指出,衛福部疾管署歷次疫苗採購文件,均未見採購價格分析資料或依據,且部分採購文件保密期限長達30年以上,應研議於不違反保密條款下,適時公開疫苗採購情形,讓資訊公開透明;而監察院指出,衛福部應檢討新冠疫苗相關採購文書設定為「密」的必要性,但相關單位仍一再拖延,其中是否有什麼不能公諸於世的內容,很難不讓人起疑。邱臣遠表示,在稍早的記者會中,行政院長陳建仁已確定將於9日到立法院進行專案報告。據此,民眾黨團將針對高端的黑箱疑慮,向陳建仁院長提出質詢,同時呼籲執政黨儘速公開高端採購合約內容,以釐清真相。

廖偉翔質疑高端疫苗採購 疾管署:絕無不法
國民黨立委候選人廖偉翔日前公布高端疫苗董事會及審計會流出的三份現場錄音檔,並有人轉述成大醫師說政府「穩過的,一路開綠燈」。針對廖偉翔持續對高端COVID-19疫苗採購案提出質疑。對此,疾管署今(2)日表示,有關檢方偵查相關案件共63案都以「查無不法」簽結,顯示政府無涉及任何不法情事。國民黨立委候選人廖偉翔近期猛攻高端COVID-19(2019冠狀病毒疾病)疫苗採購案,並提出3段疑為高端內部董事會及審計會的錄音檔,提及疫苗價格及「一路開綠燈」字句,音檔中甚至提到:「疫苗價格不能低於新台幣700元,其他都能當獎勵、全部拿到董事會。」衛生福利部疾病管制署副署長羅一鈞今天下午在例行疫報中再度嚴正澄清,強調依法採購及審查COVID-19疫苗,絕無外界質疑「一路開綠燈」情事。羅一鈞表示,疾管署在民國111年11月14日即以新聞稿公開說明,高端疫苗單劑量採購數量為200萬劑,每劑價格為新台幣881元;多劑量採購數量為280萬劑,每劑價格810元。均較BNT、莫德納的採購單價為低。此外,食藥署也在110年7月23日,以新聞稿公開說明國產疫苗審查無行政瑕疵,台灣對COVID-19疫苗緊急使用授權(EUA)審查基準及應具備的技術性資料要求,於109年10月14日即經專家會議討論後定案,並於廠商啟動第二期臨床試驗前,提供審查資料查檢表供其參照執行。疾管署強調,高端疫苗於110年10月27日獲選加入世界衛生組織(WHO)團結試驗,高端疫苗於真實世界接種的保護效益資料亦於112年12月28日被國際期刊Emerging Infectious Diseases接受,可佐證高端疫苗具有保護效益。疾管署重申,針對COVID-19疫苗採購與接種推動,均秉持專業且以全民健康福祉為優先,一切依法行政,絕無涉炒股或其他不法之事,有關檢方偵查相關案件共63案均以「查無不法」簽結,顯示政府無涉及任何不法情事。如有任何不法事證請提告,違法事項絕對依法徹查、嚴正法辦,絕不寬貸。

Novavax預計12月抵台開打 莊人祥曝:供貨50萬劑
秋冬為流感高峰,加上新冠肺炎肆虐,國內已開放6個月以上全民接種莫德納XBB疫苗,但外界對於mRNA製程疫苗有所疑慮,對此,疾病管制署署長莊人祥表示,Novavax的XBB疫苗已經在10月下旬送食藥署進行緊急使用授權審查,快的話12月可送抵台灣開打,預計提供約50萬劑疫苗。莫德納XBB.1.5疫苗自9月26日起分三階段開放接種,首周提供65歲以上民眾,以提升免疫保護力,降低重症和死亡風險;接著在10月2日開放醫護人員接種,10月9日開放6個月以上全民接種;統計至7日為止,已經接種45.9萬餘劑,而以往接種新冠疫苗,除了mRNA製程的莫德納疫苗外,還有次單位蛋白疫苗如Novavax可供選擇,但新一代XBB.1.5疫苗是否有mRNA以外的疫苗可打?《ETtoday新聞雲》引述疾病管制署署長莊人祥說法,Novavax的XBB疫苗已經在10月下旬送食藥署進行緊急使用授權審查,如果過程順利,12月可送抵台灣並開打,依據Covax採購合約,預計提供約50萬劑疫苗。另外,疾管署日前提到,Novavax的XBB.1.5疫苗已完成三期臨床試驗,準備送我國食藥署審查;美國食品藥物管理署則已在10月初通過Novavax的XBB.1.5疫苗緊急使用授權,可用於12歲以上民眾施打。
中研院士不忍了!轟指揮中心淪「高端炒手」 董智森:衛福部無恥秀下線
新冠肺炎疫情流行期間,蔡政府採購國產高端疫苗引起爭議,然而就民眾告發的相關案件,檢方均以「查無不法」簽結。不過,中研院院士陳培哲痛批,政府用國家力量扶植特定公司,介入過深、動作過於積極,疫情指揮中心更淪為「股價炒手」。對此,資深媒體人董智森痛批,衛福部官員根本是無恥秀下線。中研院院士陳培哲表示,政府以國家力量扶植特定公司,是很奇怪的作法,政府介入過深、動作過於積極,除了透過滾動式審查、不記名投票協助廠商取得緊急使用授權(EUA),又花數十億元採購,失去公平、公正及科學專業的客觀性,政府成立疫苗國家隊,給人觀感卻變成幫高端開法說會,指揮中心淪為股價炒手。對此,董智森今(7日)在《庶民大頭家》節目中直言,大家最痛恨的不是民進黨包庇高端,而是為了高端阻擋其他疫苗,中間還一直放話幫忙炒股,趁機大發國難財,就像當初前衛福部長陳時中汙衊BNT疫苗在大陸分裝,後來被證實是假消息,如今高端從韓國進口流感疫苗再分裝,卻完全沒問題,衛福部無恥秀下線。國民黨前立委林郁方認為,當時負責審查高端的學者和專家,面對涉及龐大金額的採購案及全體國民健康,必須對人民負責,所以應該要記名投票,就像立法院表決重大法案時,都採記名投票,結果審查高端卻不用記名,當然會讓人懷疑;不僅如此,高端剛成立就獲得政府全力協助,股價不斷飆高,實在啟人疑竇。

疫苗委員洩「高端通過了」 台大醫師妻砸520萬買股…超慘下場出爐
士林地檢署偵辦高端內線交易案,查出食藥署疫苗審查委員劉滄梧涉嫌把高端將通過緊急授權的內線消息,洩漏給在台大醫院擔任醫師的妻子施庭芳;施女買股前還透過LINE詢問命理師「高端通過了,可不可以買」,最後以520萬元買進20張高端股票。士林地院審理後,分別依內線交易罪、洩密罪判處施女1年6月徒刑、劉男3月徒刑。檢方查出,劉男當時擔任食藥署疫苗專家審查委員會之專家委員,於110年7月18日下午,專家審查委員會建議有條件通過高端新冠肺炎疫苗之緊急使用授權,劉竟將此重大消息洩漏給妻子,施女即於翌日重大消息公開前,分批買入高端公司股票20仟股,認定劉男涉嫌洩密罪,施女涉嫌內線交易罪,均依法提起公訴。檢方表示,劉男身為疫苗審查委員,係基於職業關係而獲悉消息之內部人,然調閱資金來源、比對通訊紀錄後,難認被告夫妻倆有共犯關係;至其餘 14 名被告,均無經手或參與各該重大消息所涉之合作案、計畫案、採購案、核准案或終止案,且審酌其等買賣高端股票之交易模式,並無證據證明其等利用地位或職務以獲悉相關重大消息,而在消息未公開前買賣高端公司股票,是以,難認其等交易行為構成內線交易,而為不起訴處分。士林地院審理後,依內線交易罪判處施女1年6月徒刑,緩刑4年,需向公庫支付100萬元;劉滄梧則犯洩密罪,判處3月徒刑,得易科罰金9萬元,緩刑2年,需向公庫支付20萬元;可上訴。

新冠快篩恐有失準度? 食藥署限業者1個月內補交對「XBB病毒」性能報告
國內第四波疫情正遭遇XBB病毒侵襲,但過去所使用的快篩卻可能無法準確驗出病毒。食藥署今天表示,即日起要求國內核發緊急使用授權(EUA)的205款快篩試劑需在一個月內繳交對XBB病毒的檢測性能,如未能通過審查將不得再進行製造或輸入。台大急診醫學部主治醫師李建璋表示,快篩是新冠最重要的檢測工具,但受到病毒量和檢體品質影響,XBB輕症化、流行廣,使得偽陰性機會增加,如有接觸史和符合的症狀,但快篩卻陰性,請使用另一個廠牌的快篩重複篩檢,才不會錯過黃金時間,避免重症和死亡的發生。食藥署副署長陳惠芳指出,XBB病毒相較過去流行的BA.2、BA.5變異株,雖然主要發生變異在S蛋白,而我國核准之快篩試劑皆是以偵測病毒N蛋白為主,應不影響檢測XBB變異株之性能,不過為確保國內快篩試劑效能,仍要求廠商於7月31日前繳交性能報告。陳惠芳說,目前國內共有205張專案核准(EUA)之新冠病毒檢測試劑核准期限至明年6月30日為止,核准期間過後的產品皆不得再製造或輸入,目前已有15案向食藥署申請新冠病毒檢測試劑查驗登記,其中已有2案獲核准取得許可證。
變種病毒多!天選之人別得意 快篩越來越不準
家人染疫,自己卻遲遲沒有快篩陽,不一定是「天選之人」,也有可能是快篩不準!隨著新冠病毒變異,過去敏感度達7成的快篩,已越來越難反映感染,專家擔憂患者恐無法及時用藥,提醒有疑慮的高危險族群,即便快篩陰,也應進一步接受PCR檢測,避免淪為重症個案。食藥署也將要求業者調查,1個月內提供評估報告。台大醫院急診部主治醫師、哈佛公衛博士李建璋指出,快篩本來的敏感度就只有7成,意思是染疫者當中,只有7成可以用快篩測出,但近期已有越來越不準的現象。快篩試劑的設計偵測的是N蛋白,而多數病毒變異都發生在S蛋白,因此不需像疫苗,經歷變異就要重新設計。然而,隨著病毒變異了好幾輪,N蛋白也已累積了足夠的變異,導致快篩認不太出,現在的感染,已不能完全仰賴快篩認定。李建璋說,如今常見的情況是,一些民眾家人確診,全家都有相同的暴露,也有類似症狀,自己卻一直快篩陰,恐影響高危險族群的用藥。若為65歲以上、有慢性病、BMI高等問題的高危險族群,因有暴露史而懷疑自己染疫,即便快篩陰,也應到醫院接受公費PCR檢測,才能及早給藥。若不是高危險族群,快篩陰不必太擔心,只需接受症狀治療即可。食藥署副署長陳惠芳回應,快篩靈敏度不如PCR,建議應搭配臨床症狀綜合判斷。經搜尋國外衛生主管機關,都未有快篩受變異株影響而失準的資訊,國內也未接獲相關通報。為了解是否有失準情形,食藥署將請業者1個月內提出評估報告。另經統計有205款快篩緊急使用授權(EUA)將在月底到期,目前有15家藥廠申請正式藥證,已有2家通過。

投書質疑疫苗涉貪 學者獲不起訴
高端提告三連敗!高端繼控告《中國時報》、臉書粉專「不演了新聞台」獲不起訴後,不滿元智大學資訊管理系教授周韻采,去年投書中時「高端騙局包裹下的貪汙三部曲」一文,控告周涉嫌加重妨害信用、加重誹謗等罪嫌。台北地檢署2日偵查終結,認定周是對於可受公評之事,基於善意而為適當評論,且已盡合理查證,作成不起訴處分。周韻采針對去年11月高端疫苗的緊急使用授權(EUA)審查火速通過一事,11月5日在《中國時報》時論廣場投書「高端騙局包裹下的貪汙三部曲」,文中批評,蔡政府動用預算向高端以每劑840元台幣,購買500萬劑疫苗,共計40億台幣。之後卻因民眾施打意願低落,必須銷毀乏人問津的到期疫苗172萬劑。換言之,已施打在台灣人民身上的高端疫苗,平均每劑需花費人民納稅錢1322元。比AZ、BNT及莫德納還昂貴的國產疫苗卻無同其相等的效力,以致接種的人民得到其他國家皆不認可的「偽防護力」。周提到,蔡政府一系列護航高端的作為,令人不得不懷疑,背後的得利者到底是誰?高端可能只是白手套,幫特定人士將政府預算洗到私人口袋裡。高端向北檢控告周涉嫌加重誹謗等罪。北檢調查時,周提出相關新聞報導及衛福部新聞稿,辯稱沒有誹謗犯意。檢察官依監察院今年3月調查報告,認為疾管署所公布的疫苗資訊與實際有落差,揭露資訊有不透明之處,導致國人接觸查證疫苗相關資訊受到限制。檢察官認定,疫苗採購流程、價格是否涉及不法,均屬可受公評之事,周女在有限資訊中蒐集相關資料,已盡合理查證義務,且她是對於可受公評之事,基於善意而為適當之評論,因此罪嫌不足,予以不起訴處分。

劣偽快篩試劑流入市面案 監察院糾正食藥署
監察院調查,去年國內爆發中國大陸製的劣質快篩試劑流入市面事件,認為食藥署疏於強化EUA(緊急使用授權)審查機制,且漠視連續產品異常的警訊,不但從未通知海關,也從未抽檢該問題試劑的安全與效能等情況,在今(27)日公布對食藥署提出糾正,並要求議處相關失職人員。監察委員蘇麗瓊、王麗珍、蔡崇義調查「中國製劣質COVID-19快篩試劑偽造為美國製造輸入我國」案,指出衛生福利部食品藥物管理署輕忽美國FDA及「ACON Laboratories Inc.」連續發布關於「Flowflex」快篩試劑已有陸製偽冒品流通之警訊,除未通知財政部關務署強化邊境查驗作業外,亦疏於強化審查機制,竟續率予核准另家業者所提「同款」試劑之專案輸入許可,嗣後又從未追查該試劑流向並抽驗其安全與效能,任該問題試劑四處流竄,肇使國內在2022年6月10日爆發劣質快篩試劑事件,危及民眾健康安全,經監察院社會福利及衛生環境委員會、財政及經濟委員會聯席會議審議,在昨日通過糾正案,並決議要求議處食藥署相關失職人員。調查委員說明,食藥署於2021年核准某公司申請美國ACON的Flowflex Home Test專案輸入,該公司於2022向台北關申報試劑進口,但經海關貨物查驗發現實際進口為中國製的Flowflex Rapid Test,因此台北關以虛報貨物名稱及產地問題,移請食藥署審理。後續發現其實美國FDA早已於2022年發布警訊,內容說明Flowflex Rapid Test未經美國FDA核准;另美國ACON 公司也同年公告,該公司產有中國製造的偽品,並宣達真偽品辨識方法之訊息等情,但是食藥署並未據以強化審查機制。監委調查指出,食藥署甚至在另一家公司於111年4月26日提出「同款」試劑專案輸入申請後,於同年5月10日即快速核准通過。此外,甲公司於2022年5月13日發函食藥署,申請註銷該款快篩試劑專案輸入核准,並於該函中提醒可能有中國製試劑改換包裝偽造產地,且已於市面流通情事,但食藥署竟辯稱該公司並無提出具體事證,因此仍未進一步查處,行事顯屬消極,相關人員確有失職。另外,調查委員指出,在海關查驗方面,關務署雖已將報關人、進出口廠商等有不良紀錄者納為風險因子,以提升查驗等級,但該系統竟沒有對問題產品名稱的風險評估,輕忽報關人常會以不同公司行號進口相同貨物,在發現進口快篩試劑有偽造產地及虛報貨名情形後,後續另家公司所提「同款」快篩試劑之報關申請案,又提升查驗強度,率予全數放行,將督促關務署檢討改善。
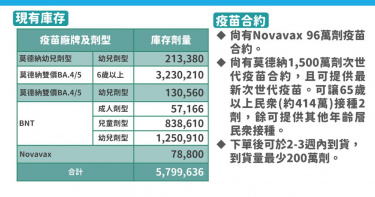
現有疫苗還有逾570萬劑 尚有次世代疫苗合約1500萬劑
中央流行疫情指揮中將在5月1日退場,外界關注是否影響疫苗的緊急使用授權(EUA)。指揮官王必勝表示,EUA到期以後,疫苗不能再專案製造、輸入,但仍可持續使用到有效期限結束為止。根據指揮中心統計,國內目前仍有579萬9636劑新冠疫苗。莫德納疫苗方面,幼兒劑型21萬3380劑、莫德納雙價BA.4/5疫苗(6歲以上)323萬210劑、莫德納雙價BA.4/5疫苗(幼兒劑型)13萬560劑;BNT疫苗中,成人劑型仍有5萬7166劑、兒童劑型83萬8610劑、幼兒劑型125萬910劑;Novavax疫苗則有7萬8800劑。指揮中心發言人羅一鈞表示,EUA期限到期前,我們會輔導業者進行正式藥證的申請。如果核准期限屆滿,沒有許可證銜接,也不影響市面上流通的產品,仍可持續使用到有效期限為止。王必勝表示,EUA到期後,產品已不能專案製造、專案輸入,但是市面上流通的、買到的,只要注意一件事,就是上面的有效期限,期限到了就不要再使用。與此同時,指揮中心尚有Novavax96萬劑疫苗合約、莫德納1500萬劑次世代疫苗合約,下單後可再2~3周內到貨。對於次世代疫苗,王必勝表示,如果有新的產品,會進口新的產品,讓脆弱族群先施打。交貨的期程已經開始談,如疫情再起,施打狀況比較需要,疫苗進來就會直接打,但若施打情況不理想,則會討論是否延後進口。藥物方面,瑞德西韋尚有9萬5548劑庫存,可用265天,尚有現貨7萬劑及開口合約4萬劑;倍拉維則又43萬8988份庫存,可用510天,尚有現貨10萬劑開口合約20萬人份;莫納皮拉韋則有7萬1212人份的庫存,可用285天,尚有現貨10萬及開口合約10萬人份。至於清冠一號,王必勝說,藥物的EUA只到明年6月底,業者在想辦法申請藥證中。

2020年成立至今 指揮中心擬5月1日解編
新冠疫情持續平穩,行政院長陳建仁今天下午2點將赴中央流行疫情指揮中心視察,下午4點由指揮官王必勝召開臨時記者會,預計說明指揮中心解編或降級規畫;據了解,具體時程可能落在5月1日。若指揮中心解編,新冠疫苗、藥物等緊急使用授權(EUA)將隨之退場,屆時如未取得正式藥證,就會正式走入歷史。專家則呼籲,台灣應將新冠防疫目標設定在「零死亡」。指揮中心自2020年1月20日報請行政院核准成立,起初以三級開設;1月23日隨即提升為二級開設,由時任衛福部長陳時中擔任指揮官;同年2月27日再度提升至最高等級、一級開設,後因陳時中投入台北市長選舉,2022年7月18日改由衛福部政務次長王必勝擔任指揮官。據了解,指揮中心向行政院建議5月1日起解編,待今天下午會議定案後,就會正式宣布。王必勝日前表示,指揮中心正在盤點最後工作,包括中重症病人的照顧流程、脆弱族群如何取得藥物、防疫物資分配、民眾衛教等。根據藥事法第48之2條,一旦指揮中心解編,現有的新冠疫苗(如高端等)及藥物(如莫納皮拉韋、倍拉維等)EUA將同步失效,須由廠商盡快申請正式藥證,或是主管機關另行訂定EUA終止時間,才能和指揮中心脫鉤。至於目前國內流通的家用快篩試劑EUA,亦會受到指揮中心解編影響。指揮中心發言人羅一鈞曾說明,部分快篩試劑EUA到指揮中心解散為止,有些則是授權到今年6月;至於市面上現有流通的快篩試劑產品,在指揮中心解散後,仍可使用到效期結束為止,大多可使用到明年或後年。台大公衛學院教授詹長權認為,指揮中心解編後需持續監控疫情,由於目前已經停止大量篩檢,建議比照國外啟動「廢水監測」,有助於在疫情重新升溫時及早發現;並持續針對住院及重症感染者檢測病毒株,以了解社區內感染情形。詹長權指出,在全面且積極善用有效充足的篩檢試劑、疫苗、抗病毒藥的前提下,應將台灣新冠防疫目標設定在「零死亡」,目前不僅歐美國家,新加坡等亞洲國家都已達成;既然已經知道國內染疫死亡的多為慢性病患、未接種疫苗者,務必採取行動,針對該族群積極預防感染、及早治療,國內應該很快就能達成「零死亡」。
高端內線交易…審查委員洩密「妻砸520萬炒股」下場慘 食藥署說話了
士林地檢署偵辦高端疫苗內線交易案,查出食藥署疫苗專家審查委員劉滄梧洩密,將緊急授權的內線消息告訴原在台大醫院影像醫學部擔任主任的妻子施庭芳,施女當天立刻傳訊問命理師「可不可以買?」並在隔天砸520萬買進20張,不法獲利15萬元。檢方將2人分別依洩密、內線交易罪嫌起訴。高端疫苗炒股疑雲鬧得沸沸揚揚,檢方調查發現,劉滄梧在2021年7月18日下午,將疫苗的緊急使用授權通過消息洩漏給妻子施女,施女得知消息後,先是傳LINE詢問命理師「高端通過了,可不可以買?」得到可以的答案後,隔天以每股260.5元新台幣買進20張高端股票,並分批在平均股價約268元的7月23日、7月26日賣出15張、5張,獲利151000元。劉滄梧將高端疫苗緊急授權通過的消息,洩密給妻子施庭芳。(圖/黃耀徵攝)檢方調閱2人資金來源、通訊紀錄,認定劉男沒有和妻子共同內線交易的犯意,依洩密罪將他起訴,施女則被依內線交易罪起訴。劉男被約談時相當錯愕,堅稱只是夫妻的隨口對談,不料妻子竟偷買股票,害他身陷官司。至於其他14名涉及高端內線交易的被告,檢方認定他們均無經手或參與各該重大消息所涉的合作案、計畫案、採購案、核准案或終止案,也無證據證明在消息未公開前買賣高端股票,因此不起訴處分。對此,食藥署長吳秀梅指出,劉滄梧參加過很多場食藥署的專家會議,而且多數都得簽署保密協議,其餘的就交由司法調查了。另外,衛福部次長王必勝透露,食藥署參與者都有保密及利益迴避同意書,這是必須簽署的,會議前也會宣讀一遍,不能洩漏訊息,否則會有民事和刑事責任,不過劉滄梧幾個月前已經向衛福部請辭,因此沒有解聘的問題。

檢調查政府帶頭炒股 衛福部早決定買高端、陳時中不斷釋利多
士林地檢署偵辦高端內線交易,清查自2020年2月起22個時段發布的重大訊息,發現衛福部食藥署、疾管署早在2021年2月間,約見高端公司人員,已訂下將採購500萬劑疫苗,時任衛福部部長陳時中不斷放出利多,士檢收案調查「政府帶頭炒股」,認為所有訊息都是事實並無炒作,未涉及不法,並未任何官員、高端公司高層。士林地檢署7日偵結起訴專家審查委員會的專家委員劉滄梧洩密罪,妻子施庭芳內線交易,不法所得15萬1000元,因主動繳回犯罪所得,建請法院依法減刑,另15人均因非內部人員獲不起訴。2021年2月全國疫苗短缺時,衛福部約見高端公司,要求準備原料、設計生產排程,同時與食藥署議約,當時高端疫苗並未通過第2期人體臨床試驗,2021年3月5日高端董事會開會要求總經理每劑不得低於700元的價格,授權與相關單位協商討論採購合約,短短3個月,股價從100元飆漲到417元,時任衛福部部長陳時中4次在媒體上放出消息。檢方整理媒體報導資料,藉以確定「重大消息」明確時點,發現衛福部2月1日約談高端公司後,高端立刻公告重訊,國產疫苗同年5月生產,6月將完成緊急授權審查,2月8日陳時中在媒體上說「大力扶植本土新冠疫苗」,並以加入「國際賽」,股價大漲至163元。陳時中更在媒體上稱「拼疫苗自給自足」,3天後,就出現消息指稱,高端首批交貨500萬劑,此時股價已經高漲到194.5元。緊接著到了3月22日媒體報導,陳時中盼總統帶頭打國產疫苗,總統府也證實總統願以實際行動支持,陳時中3月24日說出「3月底與2國產疫苗廠簽約採購」,當天股價收在249元。處分書則指,早在2月1日衛福部約見高端公司,已經洽議新冠肺炎疫苗採購,2021年5月28日晚間疾管署才以電子郵件通知高端公司雙方已應完成合約簽署,高端公司2天後,星期日晚間發布重大訊息,宣布疾管署將向高端公司採購500萬劑,而7月19日疫情指揮中心記者會公告,高端新冠疫苗透過專家審查取得緊急使用授權(EUA)。檢方表示,衛福部、高端對媒體放出的消息並無不實,另外民眾、國民黨質疑「卡疫苗」,突襲通過高端疫苗EUA、採購合約封存30年,陳時中等官員涉嫌圖利、瀆職等罪,台北地檢署共受理40多案,由3名檢肅黑金主任檢察官簽分「他字案」蒐證偵辦中。

高端內線交易偵結 食藥署審查委員夫妻起訴、基亞董座張世忠沒事!
士林地檢署偵辦多時的高端公司內線案今天偵結,士檢認為,食藥署疫苗專家審查委員會專家委員劉滄梧,2021年7月18日下午得知高端疫苗通過緊急使用授權,洩漏訊息給妻子施庭芳,施妻隔天買入高端股票20仟股,士檢認定劉男涉嫌洩密罪,施妻涉嫌內線交易罪,將兩人提起公訴。至於高端疫苗母公司、基亞生物科技董事長張世忠,張的胞妹同時也是云辰電子開發董事長的張姿玲、張的妹婿統創建設總裁黃子亮、基亞前財務長歐朝銓等人均不起訴。另外,號稱「凱基松山哥」的當沖炒手廖學邦、高端副董事長陳燦堅的好友王信雄涉嫌操縱股價部分,士檢認為無管轄權,經高等檢察署檢察長核轉台北地檢署偵辦,北檢已將廖、王2人列為偵字案被告。士檢指出,本案長期調閱資金來源、比對通訊紀錄後,認為張世忠、張姿玲其餘被告均無經手或參與各個重大消息來源的合作案、計畫案、採購案、核准案或終止案,且其買賣高端股票的交易模式,並無證據證明他們利用地位或職務以獲悉相關重大消息,而在消息未公開前買賣高端公司股票,故給予不起訴。高端炒股傳聞不斷,股價一度翻漲數倍,士檢2021年6月組成專案小組追查,調查發現,高端公司自2020年2月至2021年7月間,陸續公告利多及利空重大訊息前,疑有內線交易嫌疑,專案小組過濾投資人交易資料,並透過資金清查等偵辦作為,發現有內部人涉嫌洩漏消息予親友購買高端股票,因偵辦時機已成熟,故與母公司基亞公司所涉案件併同偵辦。本案遭外界質疑士檢長期沒動作,直到九合一民進黨敗選才重啟調查,士檢曾澄清,本案由高檢署發交和接獲檢舉資料後,檢察官認為有必要釐清,透過櫃買中心提供相關資料,反覆比對每筆資料後,還要跟櫃買中心調出特定時間交易資料進行比對,一來一回需要時間將資料詳細分析,因此並非收案1年半沒有動作。士檢今天指出,《證券交易法》禁止內線交易,旨在使買賣雙方平等取得資訊,維護市場交易之公平、公正,針對重大影響股價之消息,該署均全面清查交易時段、過濾相關公司、政府機構及百大交易人資料,查明有無不法情事,以保障投資人權益,健全市場發展。